前 言
人工智能和脑科学的交叉融合发展为机器智能与人类智能的融合提供了可能,在全球瞩目下,脑机接口技术在医疗场景的应用处在变革前夕,科学家与企业家正力争在这一科技前沿领域通过自主创新取得竞争优势。2023年9月,我国首次提出发展新质生产力这一理念,脑机接口技术作为前沿交叉学科的代表性技术,有望成为先进生产力的突破点之一。
01、 什么是脑机接口技术?其在医疗健康领域能发挥何等作用?
脑机接口(brain-computer interface,BCI)指在大脑与外部设备之间建立直接交互的通信和控制通道。现代医学对于脑电信号(Electroencephalogram, EEG)的发现和监测由来已久,随着神经科学的发展,现代医学对运动、视觉、听觉、语言等大脑功能区有了更清晰的了解。如果采集特定大脑功能区的脑电信号并加以解码和分析,则可以翻译大脑的意图及指令,从而应用于精神系统的疾病诊断以及康复治疗。在化学治疗与物理治疗之外,脑机接口技术所代表的数字治疗被视为现代医学最具前景的颠覆式创新领域之一。
脑机接口系统在医疗健康的应用短期以监测和改善为主,中期以替代为主,长期以增强为主。在一些以往较为棘手的神经类疾病中,比如:癫痫、老年痴呆、脑卒中康复、抑郁,甚至于毒品依赖等方向,脑机接口技术有望带来新的突破性的解决方案。
02、脑机接口技术分为哪些核心环节?
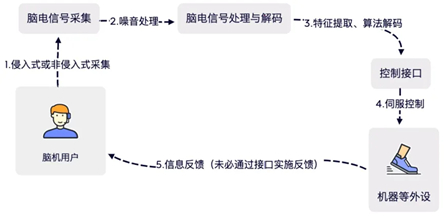
图 BCI系统示意图
在 BCI 系统中信号采集和算法解析是两个最为核心的步骤,也是 BCI 系统及产品提升有效性的关键突破点。
- 从信号采集端来看,目前市场主流的采集方式为非侵入式采集,非侵入式采集不会将电极植入大脑皮层或对用户造成其他创伤,因此安全性更高,但其取得的信号受到颅骨、皮肤等组织的干扰,会发生较大衰减,且较难精准定位到单个神经元。侵入式采集可获取皮层脑电信号(electrocortico graphy, ECoG)和单神经元记录(Spikes),与颅骨外的头皮脑电信号相比,强度、精度及分辨率都更高,对于医疗级的应用更具价值,但侵入式采集需要通过手术植入电极,且置入式电极不仅会引起排异反应也可能对神经系统造成不可逆的创伤,因此在侵入式采集的领域,如何使用微创方式或柔性电极等先进手段,降低信号采集对于人体造成的创伤是亟待攻破的技术性难题。
- 算法解析是 BCI 框架中的重要组成部分。脑电信号处理的第一步是提高信号质量,通过放大、时/频域滤波、平滑、降维等手段,突出信号特征。处理降噪后的数据将进入第二步解析阶段,即将预处理的脑信号进行特征提取,并通过算法实现对信号的解码,根据脑信号节律的分布与变化情况,得到大脑指令信息。支撑上述高质量信号处理与解析的两大关键技术是算法设计与AI 芯片。
03、脑机接口设备作为医疗器械将按照哪类医疗器械进行监管?
依据影响医疗器械风险程度的因素、以及风险程度高低两类判断标准,医疗器械可以划分为不同的种类(第 I、II、III 类)并接受不同级别医疗器械监管部门采取的不同监督管理措施(如:产品备案或注册批准等)。根据《医疗器械分类目录》的规定,BCI 设备的分类监管要求应参考如下标准:
- 任何侵入式设备基于其对人体的损伤及高风险性,应作为III类医疗器械注册;
- 对于具有增强或刺激类等辅助诊疗及或治疗功效的BCI 设备(无论是否侵入)应作为III类医疗器械监管;
- 其他一般类型的非侵入式BCI 设备应作为II类医疗器械进行监管。
目前,对于非侵入式BCI 设备已经不乏注册成功的产品及企业,对于BCI设备的III类证取证,中外的多家不同技术路线的企业已经进入了临床试验的阶段、开启在人体的数据采集处理和安全有效性验证。此外,随着BCI系统的逐步完善和标准化,后续也可能会存在针对BCI完整设备作为医疗器械整机所对应的某个核心部件的特定类型产品,通常而言,对于该等核心部件由于不会独立被病患所使用,可以考虑采取与其他整机企业合作的方式完成医疗器械注册、无需就核心部件本身单独进行医疗器械产品注册。
04、如何应对产品注册核心环节——临床试验?
根据美国食品药品监督管理局(FDA)发布的《用于瘫痪或截肢患者的植入式脑机接口(BCI)设备的非临床和临床考虑因素— FDA 工作人员指南》(“BCI 设备指南”),其中对植入式 BCI医疗器械在申请临床研究性器械豁(Investigational Device Exemption,IDE)或注册上市的预提交阶段提出了可借鉴的一般性建议,建议的主要内容包括:
临床前
- 提交对于BCI设备及其软件的完整描述、风险管理评估;
- 考虑人为因素、生物相容性、电磁兼容性等
- 验证系统与组件之间的兼容性符合特定标准并提供科学及数据依据。
动物试验
- 植入式BCI必须提交动物试验以评估体内安全性;
- 动物试验的结果能否作为设备安全性的有利证据;
- 试验方案是否已经尽可能降低动物负担或避免额外试验;
- 试验行为是否符合GLP标准。
临床试验
- 申请者应考虑设备的应用场景并于临床协议中具体描述如何执行;
- 试验面对的患者群体范围应根据潜在益处大于风险的原则结合患者需求及风险承受能力考虑;
- 试验知情同意书和试验计划内容必须具备BCI 设备指南特定要素。
2024年2月2日,我国的国家科技伦理委员会人工智能伦理分委员会研究编制了《脑机接口研究伦理指引》、生命科学伦理分委员会研究编制了《人—非人动物嵌合体研究伦理指引》,供相关科研机构和科研人员参考使用。根据公开报道和会议等,我国专家呼吁关注侵入式脑机设备应用于临床试验时的安全与伦理问题,包括但不限于:
安全方面
- 植入电极的手术风险和术后感染、排异风险;
- 在增强或刺激的场景下,需把控不会给神经元及神经系统带来损伤,避免患者产生不当幻觉。
伦理方面
- 读取患者的神经活动信息及潜意识是否涉及侵犯个人隐私并已经取得了相关主体授权、是否符合人类道德和社会伦理规范;
- 在增强或刺激的场景下,是否会超越自然水平从而引发社会公平性问题。
05、BCI企业是否可尝试申请医疗器械特殊审批以加快审批速度?
除按照一般流程申请医疗器械注册外,企业在满足相应条件的情况下还可以通过创新审批、优先审批、应急审批及附条件批准等通道加快审批进程,国家药品监督管理局(NMPA) 将予以优先办理技术审评及行政审批。针对BCI 医疗器械特殊性,可重点关注创新审批及优先审批。
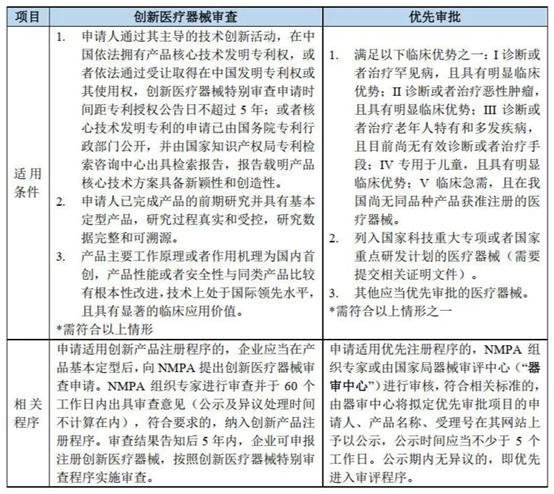
06、BCI企业在进行数据搜集和解码算法训练时应注意哪些数据合规风险?
脑机系统在算法解析阶段的核心技术 AI 算法或模型构建,需要大量相关数据进行训练,在此类 AI 医疗器械的研发过程中,其训练数据和获取及使用方式是否符合我国网络安全、数据安全及个人信息保护的相关规定同样值得关注。
就数据采集而言
训练数据的来源往往为企业直接采集(比如:企业员工数据)或通过第三方临床研究合作机构(比如:医疗机构、体检中心等)间接采集,收集数据及后续使用数据前须已获得了对应个人的同意及授权。如果涉及临床试验的,数据采集需经伦理委员会批准。在通过第三方间接采集数据时,企业与第三方的合作协议应明确约定:
- 第三方应依法征求个人有效同意收集、使用、分享及存储其相应数据,并建议第三方与该等个人约定充足的授权期间;
- 在收集后,第三方有义务应对该等数据进行去标识化的处理,数据脱敏应当明确脱敏的类型(静态、动态)、规则、程度、方法,且脱敏过程建议在第三方的经营场所或数据库中开展;
- 第三方向企业交付及分享的数据为符合前述两项要求的已脱敏原始数据库。
就数据存储和数据使用而言
企业应通过数据加密、数据隔离、访问管理、使用限制(如:不得大规模复制)、生命周期管理等方式履行网络安全与数据保护的职责。企业还应制定并完善各类内部的数据保护规范,包括但不限于《数据分级管理制度》和《网络与信息安全应急管理制度》等。
在脑机接口设备商业化推广后
器械采集的患者和医疗机构的有关数据属于医疗健康数据,建议存储在医疗机构的服务器内,不再向外传输。假设需要云计算等远程算力支持的,则应根据企业与患者和医疗机构间的合作协议,仅传输或分享已经明确授权的、脱敏后的数据。
07、BCI企业的跨境合作应注意哪些风险?
美国政府对中国在新兴技术领域实施出口管制,无论是脑机接口的信号采集设备还是 BCI 系统涉及的 AI 芯片技术均有可能被纳入到美国商务部工业和安全局(Bureau of Industry and Security, BIS)出口管制的监管范围之中。2021 年 10 月,BIS 发布了对脑机接口技术实施出口管制的意见征询文件,这是继 BIS 在 2018 年意图限制脑机接口技术出口后的第二次尝试,更令人意外的是,BIS 在去年 12 月将中国人民解放军军事科学院军事医学研究院及其下属 11 个研究所以该等机构涉及脑控技术为由纳入实体清单18,美国政府未来大概率将对 BCI 技术的出口进行更严格的限制。此外,就 AI 芯片而言,若 BCI 企业选择来自于美国的供应商或 AI 芯片设计或授权等环节与美国技术有关的,也可能在后续面临出口限令。
结合美国出口管制制度的严格规定和中美竞争日益激烈的大背景,建议脑机企业留意:
核心技术的原创性
应确保核心技术源于中国境内的企业独立研发并由中国境内的企业对核心技术展开知识产权(软件著作权或专利等)的相应布局与保护,审慎对待设立在美研发中心、与美国高校或研究机构展开合作和聘任美国专家顾问等会影响核心技术原创性的敏感问题;
核心组件的非依赖性
应确保产品的核心组件不会被境外供应商所控制,比如:可选取美国、欧洲、亚洲及境内多家核心原材料或芯片供应商,确保即使在企业自身被纳入实体清单的最坏情况下,仍能持续开展业务。
此外,对于采取跨境股权架构的脑机接口企业还应在架构设计和企业融资方面密切留意外国主体直接间接赴美投资所涉国家安全审查机制(俗称CFIUS)和美国主体对外投资所涉国家安全审查机制(俗称Reverse CFIUS)的相关影响。
08、脑机接口医疗器械的间接销售应预防哪些风险?
由于医疗器械行业的终端客户涵盖了各级医疗机构(如综合医院康复科室、康复医院、 康复医疗中心、康复门诊等)、残联系统(如残疾人康复机构)以及民政系统(如福利院、养老机构)等专业机构,基于医疗器械领域,尤其是康复治疗领域 B 端客户多且分散的特点,该行业往往均存在较高比例的间接销售收入,即企业通过经销商进行对外销售。
间接销售的模式的优势在于拓展营销渠道、节约销售成本,但间接销售也会带来如下法律风险:
经销可能缺乏资质
企业应确保经销商具备经营医疗器械的相关资质,对于第二类医疗器械而言,经销商应当向所在地设区的市级负责药品监督管理的部门备案。企业还应当定期核查经销商的相关经营许可或备案是否仍在有效期内,除资质外,经销商的经营业绩情况、履约回款情况及口碑诚信等等也应纳入经销商准入管理的考虑范畴。
需要预防经销商的商业贿赂行为
企业应尽可能避免经销商及其销售人员在产品销售过程中发生商业贿赂行为或者获取不当商业利益,具体而言,企业应与经销商签署《反商业贿赂承诺书》并制定预防商业贿赂的相关内部规范,如《经销商管理流程》《经销商行为准则》《销售合同和订单管理程序》等,并通过经销商培训等方式对这些反商业贿赂规范进行充分宣讲。为避免利益输送,经销商及其销售人员不应在企业或者终端医疗器械采购方任职或者持股。对于经销商的对公正常返利可采取抵扣后续采购款项的方式进行、不得转入任何第三方或者个人账户。





























